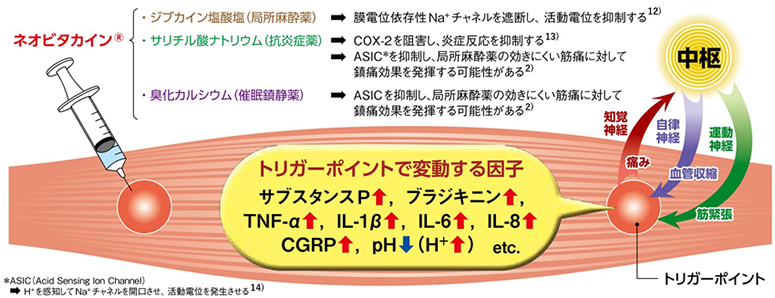
トリガーポイントに関与する因子
トリガーポイントに関与する因子を知ることはトリガーポイント注射の薬液選択に役立ちます。
とはいえ、トリガーポイントの病態は完全に解明されておらず、病期(急性期か慢性期か)や
原因により、関与する因子の重みは異なる可能性が高いと考えられます。
トリガーポイントに関与する因子
トリガーポイントは、運動神経、知覚神経および自律神経の各神経的要素に加え、多数の炎症性メディエータや発痛物質、神経成長因子のような化学分子的要素が絡んだ複雑な病態を呈します。とはいえ、トリガーポイントの病態は完全に解明されておらず、病期(急性期か慢性期か)や原因(筋損傷か精神的ストレスか)により、関与する因子の重みは異なる可能性が高いと考えられます。例えば、損傷等が起点となった急性期のトリガーポイントでは、炎症反応による知覚神経的要素の関与が大きいかもしれません。精神的ストレスにより悪化したトリガーポイントでは自律神経的要素の関与が大きいかもしれません。それぞれの要素を理解し、薬液の特徴とつなぎ合わせることで、トリガーポイント注射が高い有効性を発揮する理由も明らかになります。
トリガーポイントの運動神経的要素
Simons らは、トリガーポイントの中心的な病因部位として、運動終板(神経筋接合部)を挙げています。運動終板では運動神経が筋線維とシナプス結合しており、神経伝達物質としてアセチルコリン(ACh)をシナプス間隙に放出します。筋細胞膜に存在するリガンド依存性カチオンチャネルであるACh受容体に、AChが結合するとチャネルの開口およびNa+の細胞内流入、K+の細胞外流出が起きます。その結果、筋細胞膜に微小終板電位が発生し、微小終板電位が十分な大きさになると、筋細胞膜上の膜電位依存性Ca2+チャネルが開口し、Ca2+が細胞内に流入することで発生した活動電位は筋細胞膜を伝わり、T管に存在するリアノジン受容体を介して、筋小胞体よりCa2+の流出が起きます。このCa2+の流出が細胞内Ca2+濃度を急激に上げることで、ミオシンフィラメントとアクチンフィラメントの滑り込みを惹起し、筋は収縮します。シナプス間隙にはAChエステラーゼ(AChE)がコラーゲンQをスキャホールドタンパクとして常駐し、AChの分解に寄与することでACh濃度を調節しています。したがって、AChEの機能低下は筋収縮および弛緩に影響を及ぼす事が考えられます。AChEのmRNAはスプライシングの過程で、AChE分解能の劣った変異型を生成することがありますが、その変異型は精神的ストレスや肉体的ストレスにより誘導されうるため、ストレスはトリガーポイントにおいて重要な役割を担うことが推察されます。
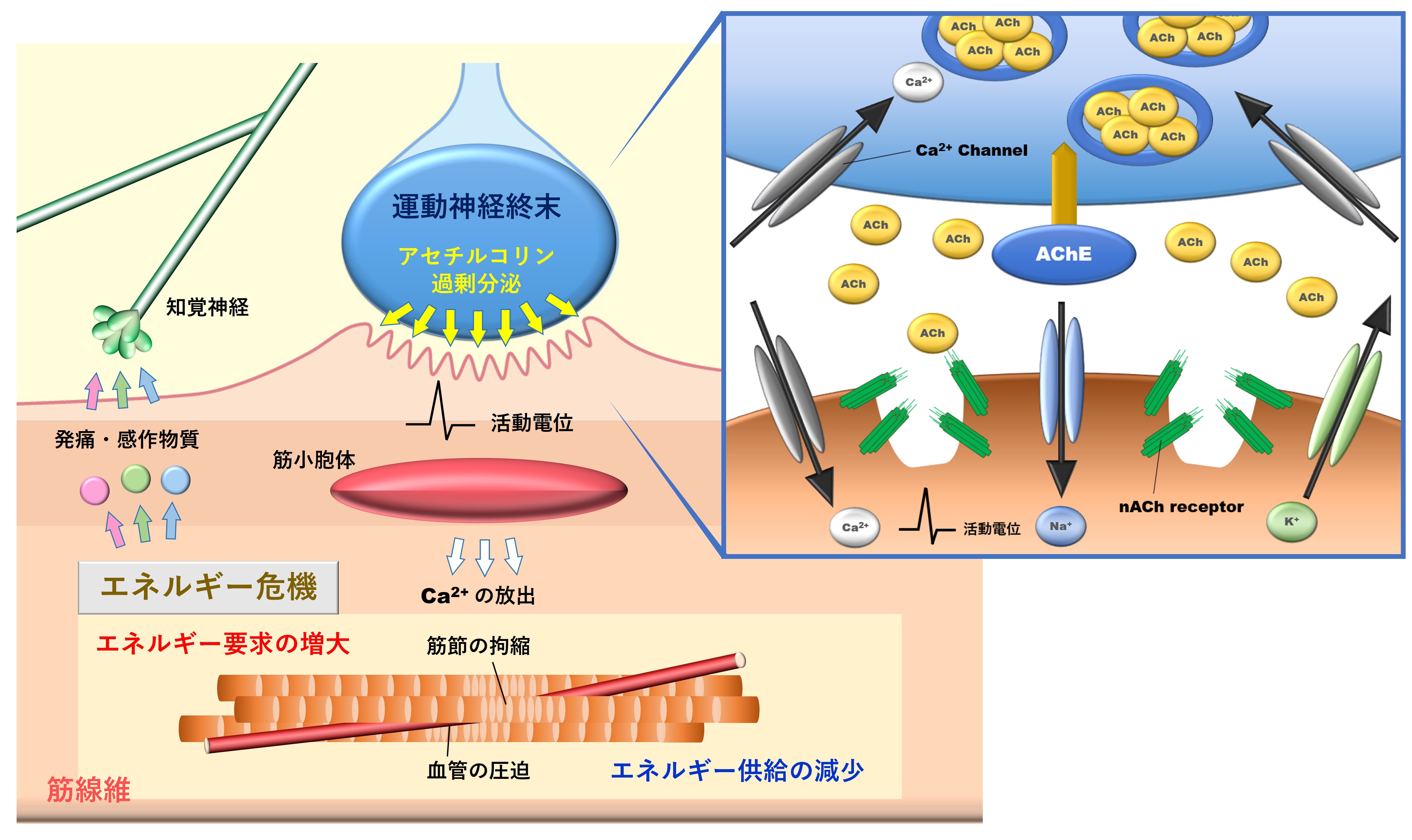
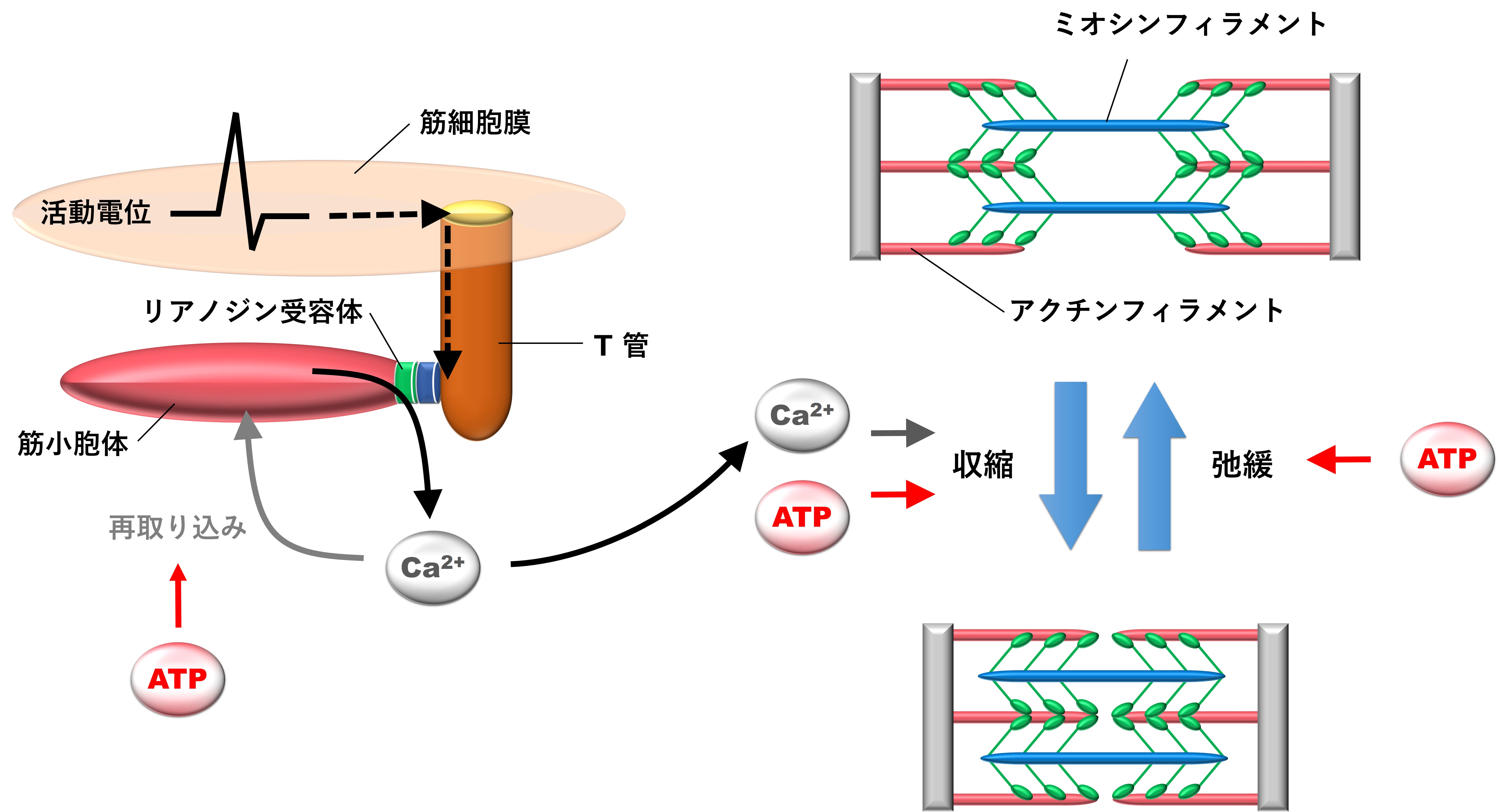
トリガーポイントの運動神経的要素において、エネルギー危機が中心的な役割を担います。運動神経機能亢進による筋収縮は知覚神経を圧迫することにより分子の軸索輸送を減少させるので、通常、ACh放出を抑制させます。一方、筋収縮により血管が圧迫されることで局所への酸素供給は減少し、筋収縮が引き起こす代謝要求の増加と酸素供給の減少はATPの分解およびATPの供給不足を引き起こします。このエネルギー危機では、前シナプスにおいて、AChの放出を直接的に抑制するATPの不足により、AChの放出は増大します。また、後シナプスにおいて、ATPを使って筋細胞内のCa2+を筋小胞体に再取り込みするCa2+ポンプは、ATPの不足によりその機能を発揮できず、Ca2+の上昇を引き金とする筋収縮を解除できません。また、アクチンフィラメントとミオシンフィラメントの滑り込みはATPを用いて解除されます。このような理由から、ATPが不足するエネルギー危機では、筋・筋膜の環境は悪循環に陥ります。
トリガーポイントの知覚神経的要素
トリガーポイントの知覚神経的要素において、現れる症状は痛みです。トリガーポイントでも、刺激を侵害受容器が感知することにより活動電位が発生し、Aδ線維およびC線維によって脳へ伝導・伝達されます。痛みを引き起こす侵害刺激因子としては、多数の化学分子、機械刺激および熱刺激があります。K+、H+および活性酸素(フリーラジカル)はエネルギー危機により過剰に発生します。他にも、ヒスタミンやセロトニン、ブラジキニンが重要な役割を担います。これらの化学分子、機械刺激および熱刺激が侵害受容器を刺激することで、カチオンチャネルは開口し、活動電位が発生します。また、組織損傷により、侵害受容器の感受性を高める感作物質が発生します。感作物質として、プロスタグランジン、ロイコトリエンおよびサブスタンスPなどがあります。感作物質は神経線維の活性化閾値を下げる(すなわち、侵害受容器の感受性を上げる)ことで、弱い刺激でも活動電位が発生するようになります。実際、活動性トリガーポイントにおけるH+、ブラジキニン、セロトニン、サブスタンスP、ノルエピネフリン、カルシトニン遺伝子関連ペプチド、TNF-αおよびインターロイキン1βの上昇が報告されており、また、MPSを想定した動物実験モデルでは神経成長因子(nerve growth factor ; NGF)の関与が指摘されています。これらの因子は、Na+チャネルの発現増加とリン酸化等の化学的修飾により活動電位の発生頻度を増大させ、トリガーポイントにおける侵害受容器の感受性を上げることが考えられます。末梢知覚神経における持続的な活動電位の発生は、中枢神経系の可塑的変化(中枢感作)を惹起し、慢性痛の原因となります。
トリガーポイントの自律神経的要素
トリガーポイントの自律神経的要素において、各部位のトリガーポイントに共通する現象は、局所の発汗、血管収縮(拡張)および立毛などですが、頭部や頚部にトリガーポイントがある場合、涙液、鼻汁および唾液の過剰分泌のような症状も発生します。骨格筋内の血管に作用する自律神経は血管縁に存在し、筋紡錘内の錘内線維間に終止します。自律神経はノルエピネフリンを放出し、錘内筋線維におけるα1受容体を活性化します。α1受容体の活性化は筋線維の長さを調節するフィードバック機構を抑制して運動機能に悪影響を与え、エネルギー危機に寄与する可能性があります。実際、運動終板における微小終板電位の振幅と持続期間をノルエピネフリンが増大させるという報告があり、トリガーポイントにおける自発的な活動電位は、α1受容体アンタゴニストであるフェントラミン、フェノキシベンザミンおよびジフェンヒドラミンにより減少するという報告があります。また、自律神経系はトリガーポイントの形成に間接的に寄与します。すなわち、機能異常をきたしている内蔵を支配する自律神経は、その内蔵より発生する電気シグナルを脊髄後角に伝達します。脊髄後角への慢性的なシグナル入力は脊髄レベルでの中枢感作を形成し、中枢感作の形成は異所性発火およびエファプスによる近傍自律神経とのクロストークを加速させます。
トリガーポイント注射の効果
トリガーポイント注射による臨床効果は、これらの神経活動の過剰興奮を末梢においてリセットし、正常化させることであると考えられます。トリガーポイント注射に使用する薬物の作用が切れれば、トリガーポイント注射の臨床効果も切れて元の症状に戻ると思われがちですが、これは間違いです。異常な筋・筋膜の環境をリセットし、正常に戻すための治療という理解が必要です。
ピックアップコンテンツ
トリガーポイントとは
トリガーポイントについての基礎的な理解から一般的な治療方法まで幅広い情報を掲載しています。初めて学習される方からご専門の先生まで、是非ご一読いただけますと幸いです。

手技動画ライブラリ
すぎはら整形外科 杉原 泰洋 先生の手技動画集です。

好発部位の解説
トリガーポイント注射の対象となる筋肉は非常に多く存在します。治療頻度が特に高い部位、筋肉について解説しています。

トリガーポイント注射の薬剤選択と作用機序
トリガーポイント注射に使われる薬液について解説し、トリガーポイント注射の作用機序を説明します。

セミナー・講演会のお知らせ
トリガーポイントに関連するセミナー・講演会の情報を掲載しています。